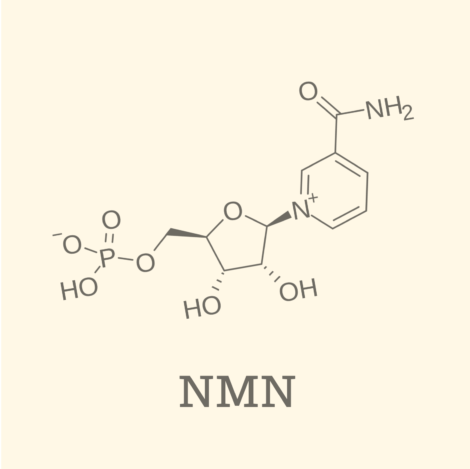
最近幾年、NMN(β-煙酰胺單核苷酸)。環繞全球的監管環境正在發生變化。特別是在美國和日本,已經發現了一些重要的發展,這些發展對食物補充品市場以及 OEM 製造和原料供應策略有直接的影響。
本文將概述這兩個國家截至 2026 年應注意的最新趨勢,希望對於考慮在國外製造或銷售 NMN 營養補充品的公司而言,瞭解這些法規將有助於產品設計。現在我們將解釋 2026 年第一季的趨勢。
アメリカ:従来の医薬品扱いから、サプリメントとしての扱いに
FDA 官方立場。
2025 年 9 月 29 日,美國食品藥物管理局 (FDA) 發佈了一份有關處理 NMN 的官方立場。內容如下:NMN 並非自動排除在「膳食補充品」定義之外這就是所謂的
2022 年左右,業界普遍認為 NMN 不能作為膳食補充品銷售,因為它是藥物研究的主題。這次的宣佈被認為是該趨勢的重大轉變。
FDA 引用 NMN 已在美國作為膳食補充品銷售的事實,以及對藥物排除條款 (DEC) 適用條件的重新評估,作為此決定的背景。這為包括 NMN 在內的膳食補充品重返市場創造了有利的環境。
遵守 NDI 通知系統。
用於在美國銷售 NMN 補充劑、新膳食成分 (NDI) 通知系統。由於 NMN 是一種相對較新的原料,製造商和原料供應商越來越多地提交 NDI 通知 (NDIN),並將安全資料和製造過程資訊通知 FDA。
須保留的證據
在美國市場,以及銷售的可用性、維持什麼證據基礎?將被強調。要求供應商及銷售通路確認的重點如下
- 控制原材料的來源、純度和雜質
- 穩定性測試的狀況。
- 符合 GMP 的製造系統
- 標籤的一致性。
當希望透過 Amazon 等電子商務通路或零售分銷進行銷售時,品質認證與合規措施的可用性也往往會影響採用決策。
差異點。
有鑑於此,美國市場的差異化因素包括
- NDI 通知提交的狀態。
- 原料生產方法(例如發酵法、化學合成法)
- 純度與品質控制 (COA/GMP)
- 標籤和廣告用語的一致性。
此規範安排導致 NMN 補充品的重新推出並擴大電子商務的銷售。對於考慮 OEM 製造或原物料供應的公司而言,在符合 NDI 規範的基礎上管理產品設計、品質文件和吸引人的表達方式是一個重要的議題。
日本:發酵產生的 NMN 安全性評估的進展。
2026 年 2 月 4 日,食品安全委員會使用特定微生物菌株 (STC2208) 生產的β-NMN。安全評估的結果已發佈在
在此評估中,即使是使用基因改造微生物的生產製程,如果最終產品是高度純化的話、可證明與傳統食品成分一樣安全決定:
從 NMN 原料作為「功能性食品」提交的數量來看,其用途也在不斷增加,國內市場的機會也在不斷擴大。
OEM 開發的重點
鑒於美國和日本各自的監管趨勢,在開發 NMN 產品時需要特別注意以下幾點。
- 美國:根據 NDI 通知和標籤合規性進行產品設計。
- 日本:確認原材料的安全性及其與標籤的一致性
- 通用:確保原料生產過程的透明度,例如發酵產生的 NMN
- 出口支援: 品質管理系統,包括符合 GMP 規範和分析證書 (COA)。
預期 NMN 市場將持續成長,而原料品質與法規遵循是決定 OEM 公司競爭力的因素。在考慮海外銷售時,企業不僅需要製造能力,還需要一個能夠在瞭解法規的基礎上,持續處理原料選擇、文件準備和標籤設計的系統。
對於那些考慮 OEM 生產 NMN 補充劑的人。
ZaaZ Ltd 提供 NMN 營養補充品 OEM 製造的諮詢服務。我們可以根據您的目標提出產品開發建議,包括配方設計、原料選擇、生產批次和包裝規格。如需更多資訊,請隨時與我們聯絡。
聯絡我們